Claisen 酯缩合反应
中文: 克莱森酯缩合反应 重要程度: ⭐⭐⭐
简介
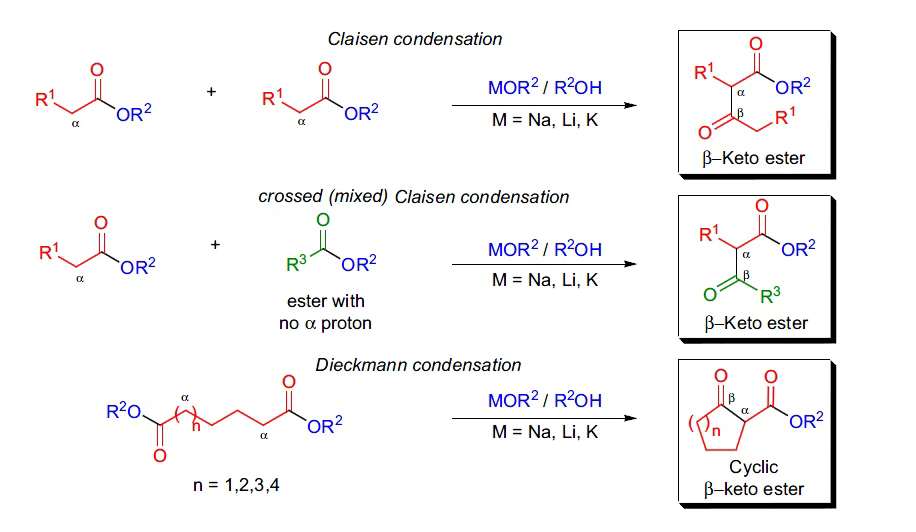
在强碱作用下,含有α-H的酯和另外一分子相同的酯缩合得到β-酮酯的反应被称为Claisen缩合反应。如果发生分子内的酯缩合反应关环,则被称为Dieckmann缩合反应。
两种不同的酯在此条件下缩合被称为交叉Claisen缩合反应。
交叉Claisen缩合可能会生成四种不同的缩合产物,因此做此反应时通常会选择一个无α-H的酯(如苯甲酸酯,甲酸酯或草酸酯)作为底物。控制好加料顺序,无α-H的酯只作为受体,这样就只生成一种产物。反应至少需要一个当量的碱(通常为醇钠,LDA或NaH),当醇钠作为碱时,醇钠的醇最好和酯的醇相同,以减少发生酯交换反应。
机理
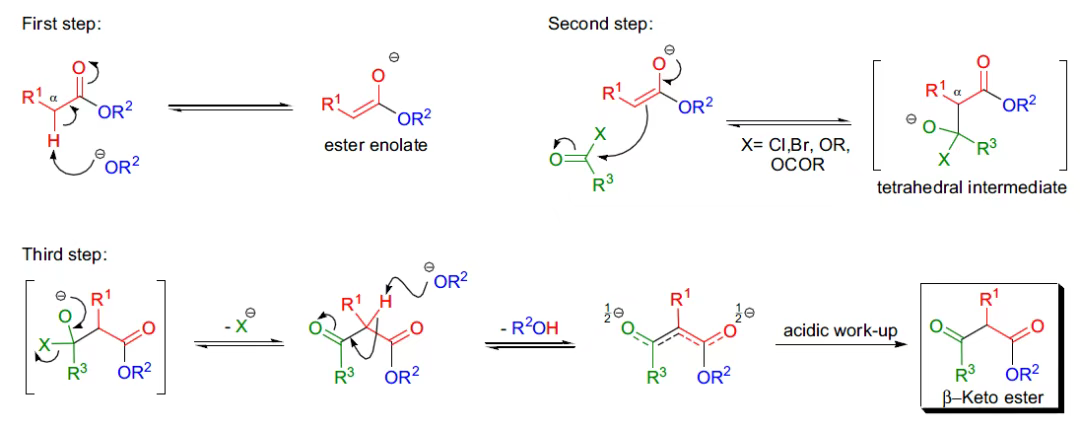
首先,碱脱去酯α-H得到酯烯醇盐,作为亲核试剂进行下一步反应;接着,烯醇盐进攻酯(或者酰氯,酸酐)的羰基,生成季碳四面体中间体;最后,离去一个烷氧基或卤素生β-酮酯。由于两个羰基之间的碳上有质子,其酸性很强,在此碱性条件下很容易脱质子生成一种共振稳定阴离子,此阴离子反应活性低于第一步的酯烯醇盐,因此不会进一步反应。
特点
此反应有三种变体:
一、酯的烯醇盐和醛酮反应可以制备β-羟基酯(类似羟醛缩合);
二、醛酮的烯醇盐和酯反应可以生成 1,3-二酮;
三、酯的烯醇盐和酰氯反应生成β-酮酯。
这三种变体都被称为Claisen缩合反应。
注意事项
两个以上的alpha- H易缩合,而一个的需要强碱
相关案例
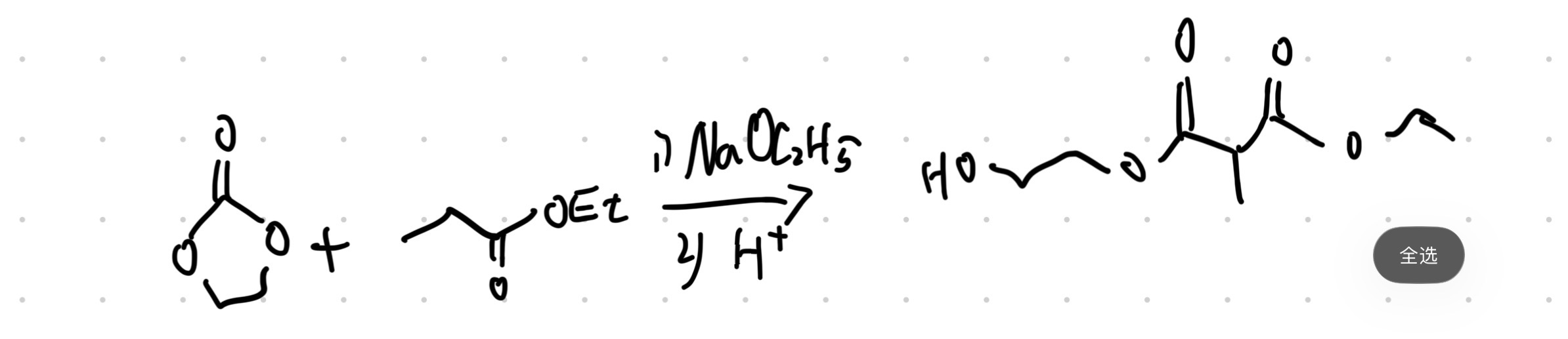
非标准克莱森缩合(酰氯充当了酯)
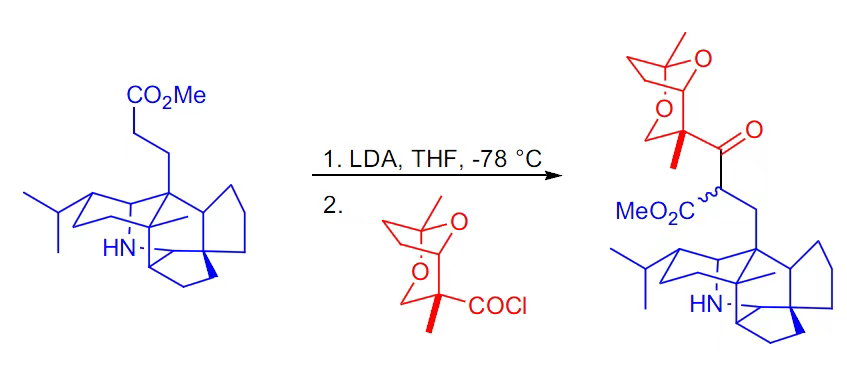
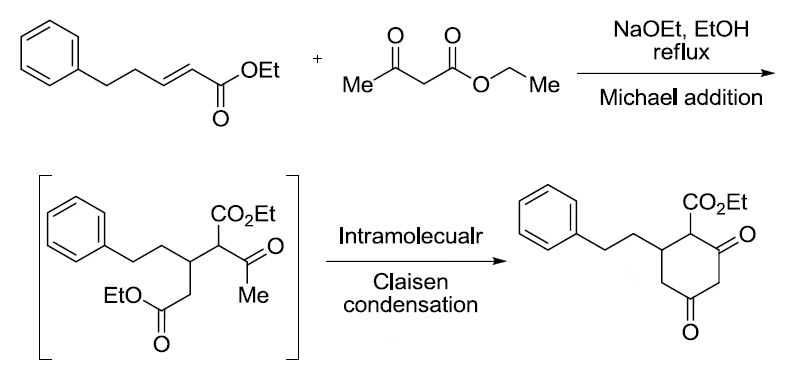
综合性和成:
Rainer Ludwig Claisen (1851-1930)生于德国科隆,他在有机化学史上可谓师出名门。在他独立进行研究之前曾经师从凯库勒,维勒,von Baeyer和Fischer 。
缩合反应关系总表:
| 分类 | 羟醛缩合 | 羟醛缩合 | 羟醛缩合 | 羟醛缩合 | 酰烃基化 | 酰烃基化 | 活性亚甲基 | 活性亚甲基 | 酯的缩合 | 酯的缩合 | 芳香醛参与 | 芳香醛参与 | 氰基参与 | 其他类烯醇缩合反应 | 其他类烯醇缩合反应 | 其他类烯醇缩合反应 | 其他类烯醇缩合反应 | 叶立德介导缩合 | 叶立德介导缩合 | 叶立德介导缩合 | 金属介导缩合 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 名称分类 | 自身缩合 | 交叉缩合 | 交叉缩合 | 定向缩合 | 烃基化反应 | 酰基化反应 | Knoevenagel反应 | Stobber反应 | Claisen反应 | Claisen反应 | Perkin反应 | Benzoin(安息香)缩合 | Stetter 反应 | Mannich反应 | Michael加成 | Darzens反应 | Morita-Bayliss-Hillman反应 | 磷叶立德 | 磷叶立德 | 硫叶立德 | Reformatsky反应 |
| 细节分类 | Aldol缩合 | Aldol缩合 | Claisen-Schmidt反应 | Mukaiyama Aldol 反应 | α-H的烷基化 | α-H的酰基化 | Knoevenagel 反应 | Stobbe 缩合 | Claisen 酯缩合反应 | Dieckmann 酯缩合反应 | Perkin 反应 | Benzoin 缩合 | Stetter 反应 | Mannich反应 | Michael加成 | Darzens 反应 | Morita-Bayliss-Hillman 反应 | Wittig 反应 | Horner–Wadsworth–Emmons 反应 | Corey-Chaykovsky 反应 | Reformatsky 反应 |
| 改进/衍生反应 | Robinson 关环反应 | Robinson 关环反应 | Robinson 关环反应 | Robinson 关环反应 | / | / | Doebner 反应 | / | / | / | Erlenmeyer-Plöchl 反应 | / | / | / | Robinson 关环反应 | / | Bayliss-Hillman反应(换成DABCO催化) | Horner–Wadsworth–Emmons 反应 | Masamune-Roushfy反应 | / | / |
| 底物 | 醛+醛/酮+酮 | 醛+醛/酮+酮 | 无α-H芳香醛 + α-H的脂肪醛/酮 | 指定 | 酯/酮/醛 + 卤代烃/苄卤/硫酸酯等 | 酯/酮/醛 + 酰氯/酸酐等 | 具有活性亚甲基 + 醛/酮 | 丁二酸酯 + 醛/酮 | 两分子酯 | 单分子酯 | 芳香醛 + 酸酐 | 芳香醛(无α-H) | 醛 + α,β-不饱和酮 | 酮/醛/硝基化合物/腈/末端炔烃/芳环化合物 + 胺 + 甲醛(或其他) | 酮/醛/硝基化合物/腈/酯类 + α,β-不饱和羰基 | 醛/酮 + α-卤代酸酯 | 醛/酮/亚胺 + α,β-不饱和醛/酮/酸/酯/腈/酰胺 | 醛/酮 + 磷叶立德试剂 | 醛/酮 + 霍纳尔试剂(膦酸酯) | 醛/酮/α,β-不饱和羰基化合物/环氧化物 + 硫叶立德试剂 | 醛/酮 + α-卤代酯 |
| 烯醇活化基团 | / | / | / | 预活化(硅基保护)/强碱(LDA) | 视情况(酯-COOR,其他需要强碱) | 视情况(酯-COOR,其他需要强碱) | -COOR, -CN, -NO2 | -COOR | -COOR | -COOR | /(酸酐提供) | / | /(氰基提供) | / | / | / | 含氮强碱 | / | / | / | -COOR |
| 反应条件 | 强碱/弱酸 | 强碱/弱酸 | 强碱/弱酸 | 强碱/弱酸 | 强碱(LDA/醇钠/氢氧化钠/氢化钠) | 强碱(LDA/醇钠/氢氧化钠/氢化钠) | 弱碱(胺类) | 强碱(醇钠/氢化钠/叔丁基钠/三苯基钠) | 强碱(醇钠/氢化钠/叔丁基钠/三苯基钠) | 强碱(醇钠/氢化钠/叔丁基钠/三苯基钠) | 对应的酸酯 | -CN | -CN | 弱酸 | 强碱(醇钠/氢氧化钠/氨基钠/氢化钠/叔丁基钠/季铵碱/哌啶) | 强碱(醇钠/氢氧化钠/氨基钠/氢化钠/叔丁基钠/季铵碱/哌啶) | 强碱(三级胺/三级膦) | 强碱(醇钠/氢氧化钠/氨基钠/氢化钠/叔丁基钠/季铵碱/哌啶) | 强碱(醇钠/氢氧化钠/氨基钠/氢化钠/叔丁基钠/季铵碱/哌啶) | 强碱(醇钠/氢氧化钠/氨基钠/氢化钠/叔丁基钠/季铵碱/哌啶) | 锌金属活化生成有机锌试剂 (R-Zn-X)以及弱碱 |
| 产物 | β-羟基羰基化合物 | β-羟基羰基化合物 | β-羟基羰基化合物 | β-羟基羰基化合物 | α-烃基化酯/酮/醛 | α,β-不饱和羰基化合物 | γ-酮酯 | β-酮酯 | 成环的β-酮酯 | α,β-不饱和羧酸 | 安息香及其衍生物 | 1,4-二羰基化合物 | β-氨基酮(Mannich碱) | 1,5-二羰基化合物(狭义) | α,β-环氧酸酯 | α,β,gamma-不饱和羰基醇取代物 | 烯烃 | α,β-不饱和酸酯 | 环氧化物 | β-羟基酯 | |
| 选择性 | 无 | 混乱 | 有高度选择性 | 有高度选择性 | 视情况 | 视情况 | 有高度选择性 | 视情况 | 视情况 | 视情况 | 有高度选择性 | 视情况 | 视情况 | 视情况 | 视情况(与羰基/双键均可加成) | 视情况 | 视情况 | 有高度选择性 | 有高度选择性 | 视情况 | 视情况 |
| 特点 | 醛或酮的α-H被碱夺取,生成烯醇负离子,进攻另一分子羰基化合物,最终生成β-羟基羰基化合物或α,β-不饱和羰基化合物 | 醛或酮的α-H被碱夺取,生成烯醇负离子,进攻另一分子羰基化合物,最终生成β-羟基羰基化合物或α,β-不饱和羰基化合物 | 醛或酮的α-H被碱夺取,生成烯醇负离子,进攻另一分子羰基化合物,最终生成β-羟基羰基化合物或α,β-不饱和羰基化合物 | 醛或酮的α-H被碱夺取,生成烯醇负离子,进攻另一分子羰基化合物,最终生成β-羟基羰基化合物或α,β-不饱和羰基化合物 | 酯/酮/醛的α-H在强碱作用下脱质子生成烯醇负离子。随后烯醇负离子进攻烃基化试剂,形成α-烃基化产物。 | 酯/酮/醛的α-H在强碱作用下脱质子生成烯醇负离子。随后烯醇负离子进攻酰氯或酸酐形成α-酰基化产物。 | 底物含有吸电子基团(EWG)(如-COOR、-CN、-NO₂),显著增强α-H酸性,使反应在弱碱条件下即可进行。 | 底物含有吸电子基团(EWG)(如-COOR、-CN、-NO₂),显著增强α-H酸性,使反应在弱碱条件下即可进行。 | 酯的α-H酸性较弱,需强碱催化形成烯醇负离子,发生分子间或分子内缩合。 | 酯的α-H酸性较弱,需强碱催化形成烯醇负离子,发生分子间或分子内缩合。 | 芳香醛的α-H因共轭效应酸性较弱,需特殊活化方式。(安息香缩合反应通过极性翻转实现) | 芳香醛的α-H因共轭效应酸性较弱,需特殊活化方式。(安息香缩合反应通过极性翻转实现) | 与此反应构成竞争的是1,2-加成的安息香缩合反应。但安息香缩合反应是可逆的,而Stetter反应的产物又更稳定,因此主要产物是1,4-加成产物。 | α-H被胺活化形成亚胺中间体,再与甲醛缩合。 | 烯醇负离子对α,β-不饱和羰基化合物的共轭加成。 | 烯醇负离子对卤代酸酯的亲核取代,形成环氧环。 | 在亲核性碱催化下,共轭羰基化合物(α,β-不饱和酯/酰胺/腈/酮)的α-位和碳亲电试剂(醛,活化酮,醛亚胺Michael加成受体)形成C-C键 | 由三苯基膦卤代烃在强碱作用下生成磷叶立德,其碳负离子进攻羰基碳,形成氧磷杂四元环(偶及中间体)。随后磷酸基团离去,生成烯烃或α,β-不饱和酸酯 | 由三苯基膦卤代烃在强碱作用下生成磷叶立德,其碳负离子进攻羰基碳,形成氧磷杂四元环(偶及中间体)。随后磷酸基团离去,生成烯烃或α,β-不饱和酸酯 | 硫叶立德的碳负离子进攻羰基碳,形成硫氧杂四元环。随后硫醚离去,生成环氧化物或环丙烷。 | 锌还原α-卤代酯生成有机锌试剂,后对羰基进行亲核加成。形成β-羟基酯锌盐,水解后生成β-羟基酯 |
| 进一步反应 | 脱水 | 脱水 | 脱水 | 脱水 | 可能伴有酮式消去 | 可能伴有酮式消去 | / | / | / | / | / | / | / | / | / | 水解 | / | / | / | / | 脱水 |
| 进一步产物 | α,β-不饱和醛/酮 | α,β-不饱和醛/酮 | α,β-不饱和醛/酮 | α,β-不饱和醛/酮 | 产物视情况 | 产物视情况 | / | / | / | / | / | / | / | / | / | γ-酮酸或醛 | / | / | / | / | α,β-不饱和酸酯 |