六元芳杂环的反应
重要程度: ⭐⭐⭐
吡啶N的反应(一种非常不活泼的芳香亚胺)
吡啶氮原子的亲核性,是由于氮上的孤对电子不能离域到环中。它们处在与环 p 轨道正交的 sp2道中,正交的轨道间不会有相互作用。
N酰基化反应
吡啶是对于羰基合理的亲核试剂,因而常被用作酰基化反应的亲核催化剂 (nucleophilic catalyst)
DMAP(N,N-二甲基氨基吡啶),由于氨基的给电子效应增强吡啶氮原子的亲核特性。吡啶 “催化” 的酰基化反应常常需要在吡啶溶液中进行, DMAP 的催化仅需要在其他溶剂中少量地加入便可达到同样的效果。
N溴化反应
一些溴化反应中,吡啶也可以作为亲核性催化剂参与反应:
另一种在溴化反应中使用吡啶的方式,是用稳定的晶体化合物替代危险的液溴。这个化合物,被称作三溴化吡啶钅翁 (pyridinium tribromide), 是吡啶与 Br3- 阴离子的盐。
可被用于溴化烯烃等活泼的化合物。
N硝化与磺化反应
吡啶与硝酸类的质子型硝化试剂反应全部生成 N-质子化产物, 但与四氟硼
酸硝 盐可以在氮上发生硝化反应, 获得的 N-硝基吡啶盐产物如1-硝基-2,6-二甲基四氟硼酸吡啶盐可作为非酸性硝化试剂的良好反应物, 且具有位置选择性。
吡啶与三氧化硫可在氮上发生磺化反应生成结晶性的吡啶-1-磺酸盐两性离子, 常称为吡啶三氧化硫络合物, 该络合物在热水中不稳定, 会水解成硫酸和吡啶, 可以作为温和的磺化试剂。
Cr(VI) 化合物的吡啶配合物
氮上的氧化反应
吡啶易与过氧酸反应生成 N-氧化物, 该化合物具有许多的反应性能, 而很
多吡啶相关的有制备价值的反应也是通过该化合物来实现的。相比于吡啶来说,啶的 N-氧化物的 N-氧官能团促进了α-和γ-位的亲电和亲核加成反应。而N-氧化物通过和磷 (Ⅲ ) 化物脱去氧原子重新生成吡啶。
吡啶的芳香亲电取代反应
吡啶 π 体系轨道较低的能量,在环上的亲电取代是困难的。
氮的孤对电子是碱性的,并且也是好的亲核试剂。一般的亲电取代反应,例如硝化反应的试剂,都是酸性的。
Friedel–Crafts 酰基化反应,需要 Lewis 酸催化,只有alcl3会在氮上反应。
在吡啶上的芳香亲电取代反应不是一个有用的反应。环本身就是不活泼的,并且亲电试剂还会进攻氮,使环更加不活泼。请避免使用简单吡啶上的硝化、磺化、卤代,及 Friedel–Crafts 反应。
在发烟硫酸中吡啶与溴作用可得到3-溴吡啶, 在高温条件下吡啶可在3-位发生氯代反应, 利用三氯化铝作催化剂, 可降低反应温度使得反应顺利进行。
被活化的吡啶可发生芳香亲电取代反应:
只有当吡啶中含有给电子取代基,例如 NH2 或 OMe 时,才能发生有用的亲电取代反应。
被双重活化的吡啶,就像是苯环一样被硝化。硝基在氨基的邻位和甲氧基的对位出现。
吡啶的亲核取代反应
由于氮原子的吸电子诱导效应和吸电子共轭效应的共同作用,使得吡啶不是一个好的芳香亲电取代反应的底物,却是芳香亲核取代反应的好原料:
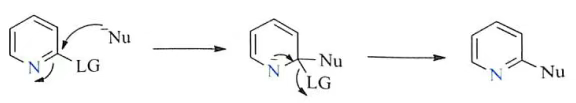
在此反应过程中,可以认为吡啶环如果有吸电子基团的取代,第一步亲核加成更容易进行;在第二步重新芳构化的过程中,离去基团的离去能力又成为了关键因素。因此,可以将此反应分为两类:①离去基团为氢负离子;②离去基团为卤素以及其他好的离去体系。
20世纪初期,A. E. Chichibabin发现.110°C下在二甲胺溶液中吡啶会与氨基钠反应,以80%的产率生成2-氨基吡啶。这就是齐齐巴宾反应(见专栏)
当吡啶环C2或C4位有好的离去基团(如Cl,Br,NO2等)时,易与亲核试剂发生芳香亲核取代反应:
例如:
2-甲氧基吡啶 的取代反应可用于合成氟吡汀 (flupirtine):
第一步是一个芳香亲核取代反应。第二步中,硝基被还原为氨基,这对吡啶环没有造成任何影响。最后,孤对电子无法离域到吡啶 N 上的那个氨基,在其他两个氨基 (胺基)的存在下被酰基化。
吡啶酮也是很好的芳香亲核取代反应的底物:
2-羟基吡啶 倾向于以“酰胺”的形式存在,因为在芳香性保留的情况下,它还利用了=O 强键提供的稳定性。每根 C=C 双键中都有两个电子,酰胺的三角型氮上还有一对孤电子。典型酰胺结构中孤对电子的离域使这一点表现得更清楚。
吡啶酮是吡啶环C2或C4位有羟基取代时的主要存在形式。当C3位有羟基取代时,主要存在的形式为:
吡啶 N-氧化物面对亲电试剂和亲核试剂都活泼
由于氧负离子的给电子效应,可以活化吡啶环以利于其进行亲电取代反应,并在给电子基团的邻、对位进行反应,这与吡啶的芳香亲电取代反应不同。
与使简单亲电取代反应发生的相同的活化作用——氧化为 N-氧化物——也能使一种有用的亲核取代反应发生。氮原子上的正电荷促进亲核进攻,氧原子还可以与 PCl3 转化为离去基团。
试剂 PCl3 同时会将羧酸转化为酰氯,而酰氯会在最后一步中被水解回去。这是一个实用的流程,因为氯原子被引入到 2 号位,这便使它可以继续被取代,例如被胺取代。
吡啶 N-氧化物吡啶 N-氧化物 对于环中相同的几个碳原子 (2-, 4-, 和 6-) 的亲电和亲核取代都是有用的。
如果 2 号位有一个烷基,那么在更远距离处的亲核取代反应,将会在与酸酐反应时发生。
这个化合物会发生重排,乙酰基迁移到侧链上,并恢复芳香性。
烷基吡啶的反应
烷基吡啶的特征性反应是与吡啶环直接相连的碳上可发生去质子化反应, 生成碳负离子。在不同溶剂中, 吡啶环上不同位置所连的侧链烷基反应性能不同,实际生成的碳负离子取决于离子与溶剂两者的平衡。在吡啶α-和γ-位上的碳负离子是更为稳定的, 由α-和γ-烷基吡啶去质子化所生成的碳负离子可进行广泛的化学反应。
由于吡啶α-和γ-位上的碳负离子的稳定性, 乙烯基吡啶和炔基吡啶可与亲核试剂发生 Michael 加成反应。
此外, 烷基吡啶的季铵盐中, 侧链上氢的酸性更强, 可在十分温和的条件下
发生缩合。
甜菜碱吡啶 盐在弱碱如 Na2CO3/H2O 作用下, 很容易发生烷基化和酰基化反应生成吡啶 化合物, 再经过还原反应消除吡啶生成酮或1,3-二酮。
六元芳杂环的DA反应
六元芳杂环可以包含氧
α-吡喃酮 相当不稳定,但吡喃酮是芳香的
吡喃钅翁 (pyrylium) 盐是稳定的芳香阳离子,以金属配合物的形式为很多花提供了颜色。
Diels–Alder 反应可以在α-吡喃酮上发生。它们也相当不稳定,几乎没有芳香性: