五元芳杂环的反应
吡咯的反应(类比烯胺来记忆)
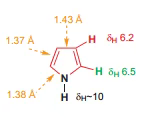
要使吡咯质子化,必须在强酸作用下才可以进行,而且质子化的位点不在氮原子上,而是在C2位上:
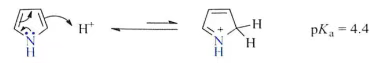
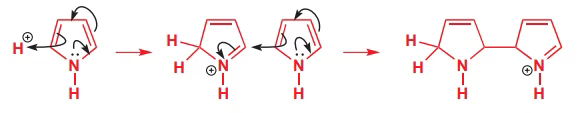
这是因为氮原子的给电子共轭效应大于吸电子诱导效应,导致其碱性减弱而环上碳原子电子云密度升高而造成的。当吡咯环上有吸电子基团时,该质子化反应更加不易发生。质子化的吡咯会加成另一个分子(烯胺aldol,,)
实际上,吡咯具有一定的酸性。
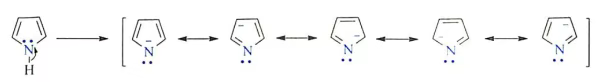
阴离子中的氮原子含有两对孤电子:一对离域在环中,另一对定域在氮原子的 sp2轨道上。较高能的后者是新的 HOMO, 也是分子发生反应的位置。N-酰基化衍生物通常可通过这种方式制取。
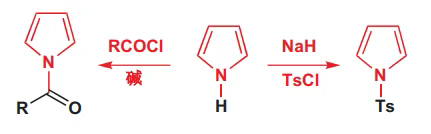
所有的离域都将电子由氮原子推向环,环上是富电子的。这意味着吡咯很容易被亲电试剂进攻。与溴单质的反应不需要 Lewis 酸,并且全部四个空位都会被取代 (验证吡咯的芳香性)。
一些反应可以得到控制,以很好地产率给出单取代产物。其中一种是Vilsmeier 反应, 反应中, N,N-二甲基酰胺与POCl3 结合,在没有强酸或 Lewis 酸的存在下制得一个碳亲电试剂。这是 Friedel–Crafts 酰基化反应的替代方法,可与芳香化合物排序中较活泼的一端的化合物 (吡咯) 反应。(详见专栏)
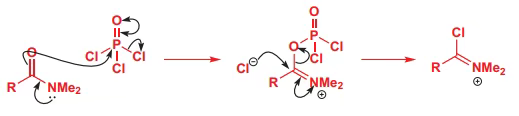
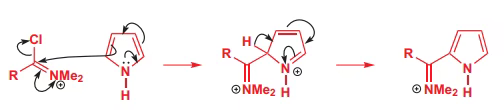
另一个很好的例子是 Mannich 反应
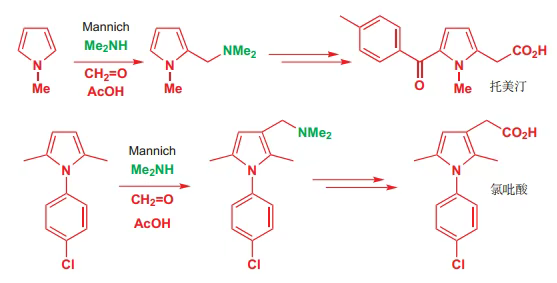
现在回到其亲电反应:
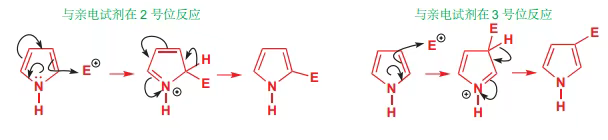
为什么喜欢在2号反应,而非3号呢?
第二种中间体是“交叉共轭的 (cross-conjugated)”,而第一种则是更稳定的线形共轭体系。
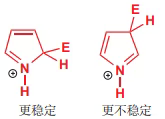
那如果我不想在2号做反应怎么办?
于吡咯上的亲电取代反应发生得太容易,可以引入一个酯基的占位基团
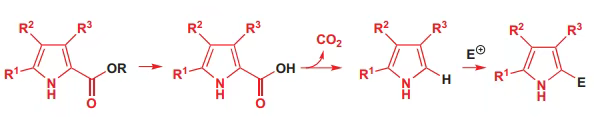
脱羧是吡咯的一个一般反应:它是一种逆向的 Friedel–Crafts 反应,亲电试剂是一个质子 (由羧酸本身提供),离去基团是二氧化碳。
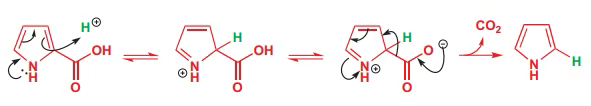
呋喃,噻吩的反应(吡咯的氧硫类似物)
用氧原子替代氮得到的呋喃 (furan), 和用硫替代得到的噻吩 (thiophene),也非常容易发生芳香亲电取代反应,虽然不如吡咯,在这三者中,氮是最强的电子给体,氧其次,硫最差。噻吩的活性与苯相当。
噻吩是这三者中活性最差的,因为硫与环上共轭的填有孤对电子的 p 轨道, 是 3p 轨道而不是 2p道 (N 或 O 上的),因此与碳的 2p 轨道重叠得不是很好。
呋喃和噻吩或多或少都会参与一般的 Friedel–Crafts 反应,选用活性较弱的酸酐 (此处是醋酸酐, Ac2O) 代替酰氯,并优选比AlCl3 弱些的 Lewis 酸。

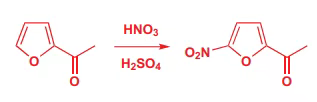
区域选择性与吡咯的相同——两种情形中 2 号位都比 3 号位更活泼。被钝化的呋喃可以被硝化。
呋喃更倾向于亲电加成(共轭二烯烃)
呋喃比吡咯的芳香性弱,相比于取代反应,它就会倾向于加成。
溴化反应以通常的方式开始,但一分子甲醇捕获了第一步反应形成的阳离子,并完成对呋喃的1,4-加成。
初期加入的溴原子现在会被呋喃氧原子推落,以得到一个相对稳定的共轭钅羊离子,继而添加第二分子的醇。
这个产物隐藏了一个有趣的分子。在环的各侧,都包含一个缩醛,如果我们将它们水解,则会得到“马来(二)醛 (maleic dialdehyde)” (顺丁烯二醛)——一个很不稳定,无法分离的分子。
可以通过氧化,得到“马来(二)醛 (maleic dialdehyde)”继而发生wittig反应:
如果将呋喃考虑为一个在环的两侧的烯醇醚,拓宽到呋喃本身, 1,4-二羰基化合物的来源上。如果呋喃中的两个烯醇醚被水解,我们便可得到一种 1,4-二酮。
包含呋喃的最便宜的起始原料是 2-呋喃甲醛 aldehyde) 或“糠醛 (furfural)”
糠醛是一种特殊的化合物,其具有一分子的醛基,可以与tollen,菲林试剂反应
在一般情况下,噻吩既可以在C2位发生质子化反应,也可以发生硫的质子化反应。但它与呋喃不同,不会因为硫的质子化而导致碳硫键的断裂开环,这被认为是与噻吩环的张力较小有关。
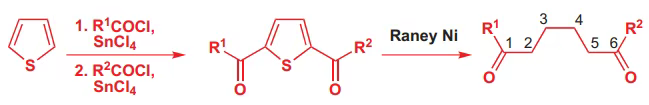
只有通过特殊试剂,如兰尼镍进行的硫原子的还原去除开环:
吡咯、噻吩,或呋喃亲核取代反应需求活化基
对于吡咯、噻吩,或呋喃,亲核取代反应是一个相对稀少的反应,都需求硝基、羰基、硫酰基等活化基。
下面例子被用于制取止痛药酮咯酸 (ketorolac)
机理
如下:进攻发生在 2 号位,是因为离去基团在二号位,也是因为负电荷可以从那个位置离域到酮上。
五元杂环的DA反应
五元杂环可以在 Diels–Alder 反应中充当双烯体。
Boc 基减弱了吡咯的亲核性,并促进了与一个炔基砜的 Diels–Alder 反应。这个反应的产物是镇痛剂地棘蛙素 (epibatidine) 合成的中间体。
呋喃尤其适合进行 Diels–Alder 反应,由于双烯体是芳香性的,因而反应是可逆的,并且得到热力学产物, 外型加合物 (exo adduct)。
噻吩环的高芳香性使其更为稳定。只有当硫原子被氧化后,噻吩环中的双烯体才可以发生Diels-Alder反应: